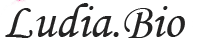NAD+(烟酰胺腺嘌呤二核苷酸)是一种在生物体内广泛存在的重要辅酶,参与调节多种生物化学反应,从细胞能量代谢到DNA修复等多个方面都发挥着关键的功能。NAD+是三羧酸循环的重要辅酶,促进糖、脂肪、氨基酸的代谢,参与人体能量的合成。此外,NAD+还是辅酶Ⅰ消耗酶的唯一底物(DNA修复酶PARP的唯一底物、长寿蛋白Sirtuins的唯一底物、环ADP核糖合成酶CD38/157的唯一底物),在生物体内的多种生理过程中发挥了至关重要的作用。

NAD+的主要作用之一是激活人体的长寿因子,通过维持端粒的长度来减缓衰老过程和延长寿命。它还有助于促进DNA的修复,延缓细胞衰老速度,并促进细胞再生,提高细胞的能量产生,从而抵抗免疫系统疾病,保持身体的健康。然而,随着年龄的增长,人体内的NAD+含量会大幅度下降,导致各种衰老症状的出现。因此,维持细胞内充足的NAD+含量对于维持机体正常功能至关重要。
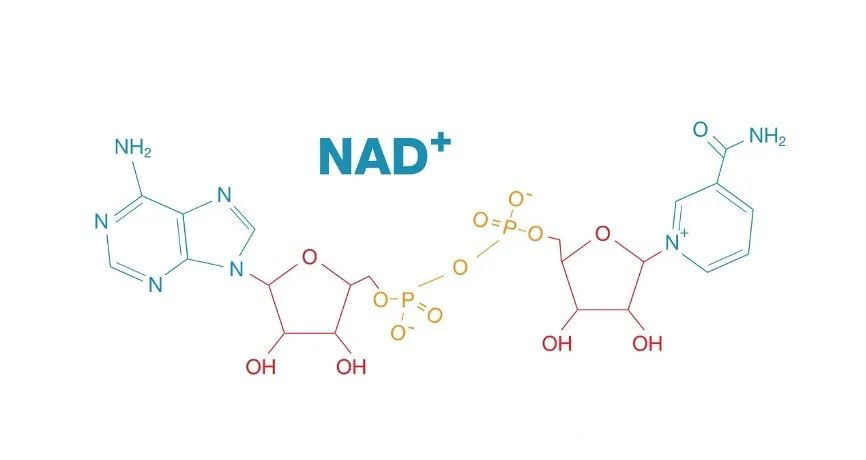
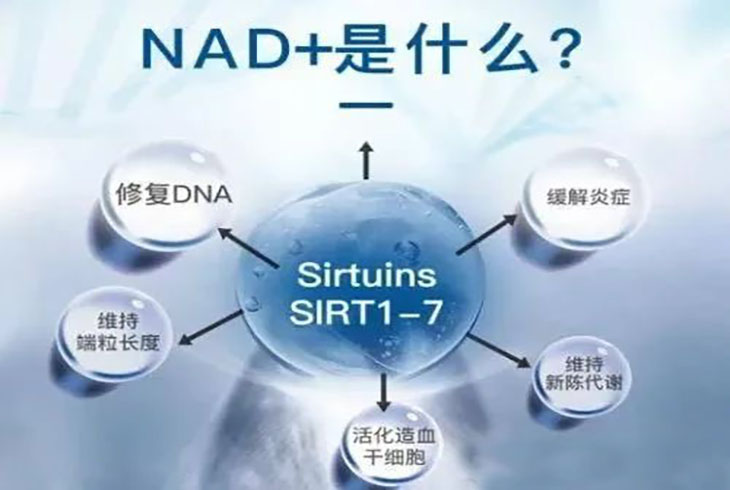
一、NAD+的分子式
NAD+(Nicotinamide Adenine Dinucleotide),全称烟酰胺腺嘌呤二核苷酸,已成为人类衰老抑制领域的关键突破。1904年,英国杰出的生物化学家亚瑟·哈登(Sir Arthur Harden, 1865-1940)首次发现并命名了NAD+,因此荣获1929年诺贝尔化学奖。这一发现犹如一枚重磅炸弹,震撼了整个衰老抑制领域,引发了广泛的科学关注和研究。众多诺贝尔奖得主,包括汉斯·冯·奥伊勒-歇尔平(Hans von Euler-Chelpin, 1873-1964)和奥托·海因里希·沃伯格(Otto Heinrich Warburg, 1883-1970),均对NAD+进行了深入探究,其历史已跨越百年。
如今,人类已对NAD+的卓越功能及其在衰老抑制中的作用机制有了深入的了解。这些宝贵的知识不仅丰富了我们的科学认知,更为临床实践和衰老抑制剂的研发提供了坚实的理论基础。
二、NAD+的功能
NAD+作为自然界中广泛存在的关键分子,从单细胞的细菌到复杂多细胞的灵长类生物,它都是细胞能量代谢调控不可或缺的一部分。在细胞的核心——线粒体中,NAD+发挥着至关重要的作用。线粒体通过一系列代谢反应产生电子,与NAD+结合后,使其转化为还原态的NADH,进而驱动能量的产生。一旦NAD+水平不足,细胞将无法有效生成能量以维持其生存和功能。
NAD+不仅有助于将食物高效地转化为能量,更在维护DNA的完整性和确保细胞功能的正常发挥上扮演了核心角色,从而保护我们的身体免受衰老和疾病的侵袭。简而言之,没有NAD+,许多生物将不可避免地面临生命活动的迅速衰退。
三、NAD +下降是老年相关疾病的重要触发因素
随着年龄的增长,NAD+水平会下降(详见图1)2。“到50岁时,体内NAD+水平大约是20岁时的一半”,该研究作者在接受采访时说道。
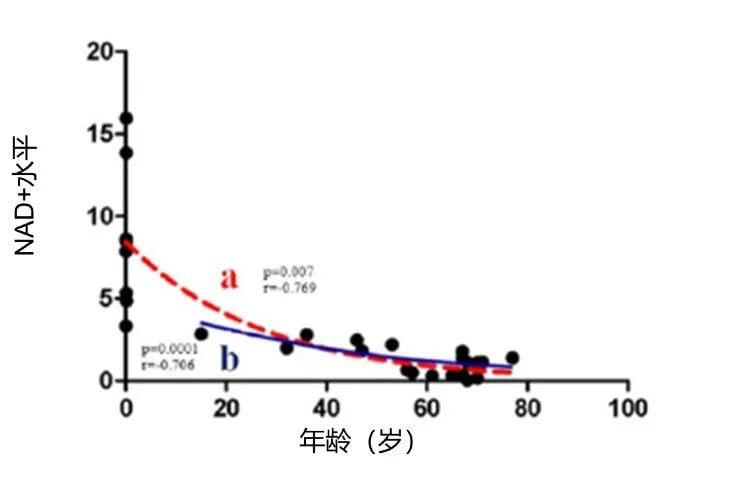
图1:NAD+随年龄增加在人体内的水平呈下降趋势2
注:红线“a”表示 NAD+水平在一生中的变化情况,而蓝色线“b”仅考虑青春期后NAD+水平的变化。
随着NAD+水平的降低,DNA修复、细胞应激反应和能量代谢调节机制会受到严重影响,这可能导致一系列与年龄相关的疾病。这些影响的具体机制可能与PARP(腺苷二磷酸核糖聚合酶)的过度激活、免疫系统功能下降以及SIRT(NAD+依赖的去乙酰化酶,也称为“长寿蛋白”)的表达下调等代谢紊乱紧密相关。
这些代谢紊乱进而可能诱导多种疾病的发生,包括但不限于肥胖、胰岛素抵抗、糖尿病、高血压、非酒精性脂肪肝、动脉粥样硬化、阿尔茨海默症(俗称老年痴呆)、视网膜病变以及抑郁症等。这些发现强调了维持NAD+水平在预防和治疗年龄相关疾病中的重要性。
四、NAD+的生物合成路径与生物合成前体
目前已知存在三种NAD+生物合成路径:犬尿酸(de novo,也称从头合成)途径、Preiss-Handler途径以及补救途径。在哺乳动物中,补救途径尤为关键,它被认为是维持细胞内NAD+正常水平的最主要合成途径(如图2所示)。
在犬尿酸途径中,NAD+源自于人体必需的氨基酸——色氨酸,这种氨基酸主要存在于肉类、奶酪、鸡蛋和鱼类等食物中。色氨酸经过酶促反应和非酶促反应转化为喹啉酸(QA),随后在喹啉酸转磷酸核糖基酶(QAPRT)的催化作用下,QA转变为烟酸单核苷酸(NAMN)。此外,NAMN也可以通过Preiss-Handler途径生成,当食物或膳食补充剂中的烟酸(NA)经过烟酸转磷酸核糖基酶(NAPRT)的催化作用时,也能生成NAMN。
在这两种NAD+合成途径中,NAMN进一步在NMNAT的催化下转化为烟酸腺嘌呤二核苷酸(NAAD),随后NAAD在NAD合成酶(NADS)的作用下最终生成NAD+。
NAD+生物合成的补救途径则与摄入维生素B3相关的天然化合物紧密相连,这些化合物包括烟酰胺、烟酸、烟酰胺单核苷酸(NMN)和烟酰胺核苷(NR)。其中,NAM作为起始分子,既来源于食物摄取也来自于NAD+消耗酶(如NAD+依赖的sirtuin、PARP、CD38等的副产物)的代谢产物。首先,NAM在烟酰胺转磷酸核糖基酶(NAMPT)的催化下转化为NMN,随后NMN再在NMNAT的催化作用下生成NAD+。
值得注意的是,NAMPT在哺乳动物NAD+合成中扮演着限速酶的角色,其表达水平会随着细胞压力(如DNA损伤、饥饿等)而呈现高度动态变化。此外,肥胖和高热量饮食均可导致多种组织内NAMPT与NAD+水平的降低。
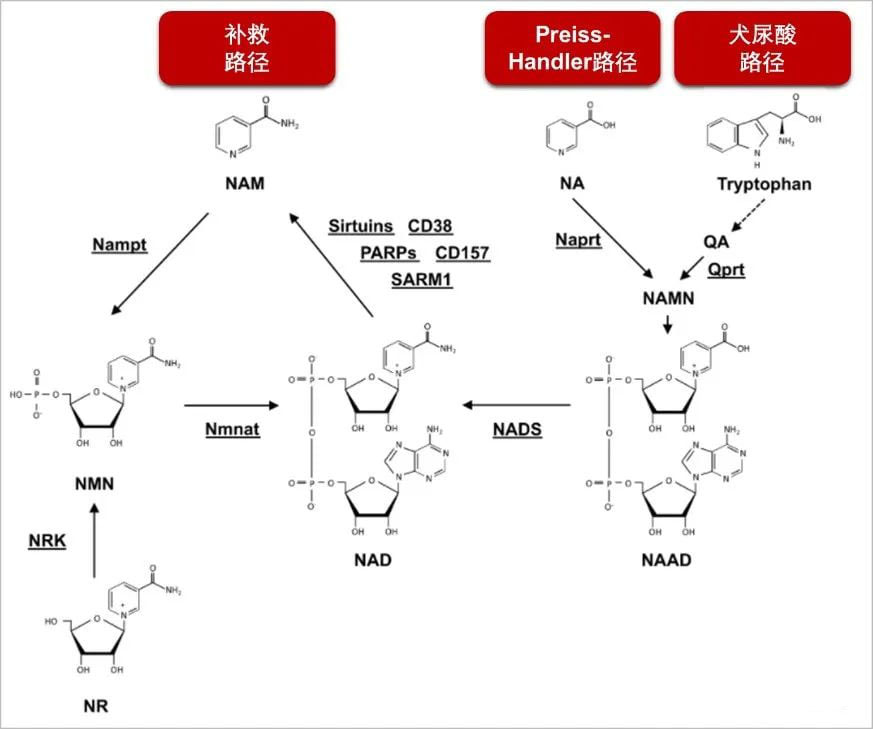
图2:NAD+在体内的生物合成路径
NAD+的前体共有五种,分别是NA(烟酸)、NAM(烟酰胺)、NMN(烟酰胺单核苷酸)、NR(烟酰胺核苷)和NAR(其他相关前体化合物,如图3所示)。
通过补充这些NAD+前体,可以有效促进NAD+的生物合成,进而提高体内NAD+的水平。因此,NAD+前体补充剂被视为一种潜在的延缓衰老和改善年龄相关疾病的治疗策略,具有广阔的医学应用前景。
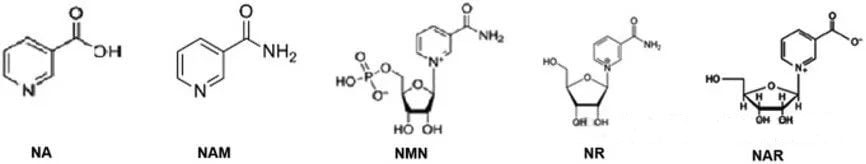
图3:5种NAD+前体的化学结构
举例来说,有深入研究表明,补充NMN(烟酰胺单核苷酸)可能通过显著提升体内NAD+水平,来预防和治疗多种组织损伤与疾病。具体来说,NMN的补充有助于减少肥胖并保护血管健康,减少神经炎症从而改善阿尔茨海默病及认知障碍,同时还能改善免疫系统的功能和肌肉健康。
目前,多数相关结论主要基于动物研究,但这一领域的研究正在逐步拓展至人体试验,以进一步验证NMN的潜在疗效。
五、提高NAD+水平对身体健康的获益
鉴于NAD+水平的降低与加速衰老、代谢紊乱、心脏病以及神经退行性疾病等紧密相关,提升NAD+水平具有显著的潜在益处。
这些益处包括但不限于延缓衰老过程、逆转与年龄相关的多种疾病(如代谢性疾病、阿尔茨海默症、心脏病以及肌肉功能下降等),进而延长健康寿命(如图4所示)。
因此,NAD+水平的提升成为科研和医疗领域关注的焦点。
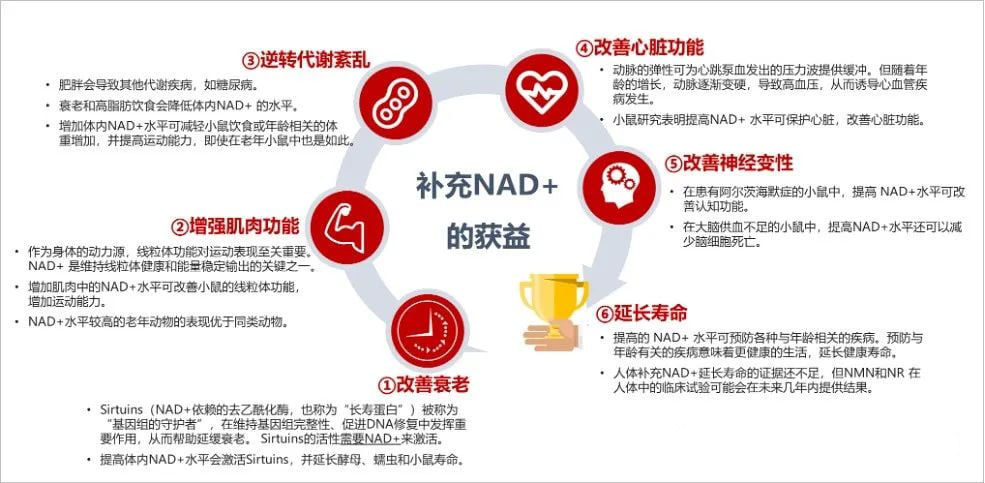
图4:补充NAD+水平的获益
六、提高体内NAD+水平的方法
NAD+水平可通过增强其体内的生物合成来提升,这主要可以通过两种途径实现:一是增强参与NAD+生物合成的酶活性,二是直接补充NAD+前体物质。
①通过培养健康的生活方式,如禁食和锻炼,不仅有益于心理健康,还能有效提升体内的NAD+水平。微生物研究揭示了热量限制能激活酵母中的NAD+依赖基因sirtuins,从而促进NAD+水平的增加。同样,在人类研究中,有氧运动和阻力运动也被证实能够恢复肌肉中参与NAD+合成的年龄依赖性酶活性。
②另一种提升NAD+水平的方式是通过补充NAD+前体,如NMN(烟酰胺单核苷酸)和NR(烟酰胺核苷)。这两种物质是NAD+的生物合成前体,它们通过NAD+生物合成的“补救途径”来增加体内的NAD+水平。
目前,人类服用NMN和NR的安全性已经得到了初步验证,未发现显著的安全性问题。
七、NAD+的未来
随着世界人口老龄化的加剧,人们享受到了更多家族欢聚的时光,然而,这也带来了老年慢性疾病的沉重负担。
据国家统计局2019年末的数据,我国65岁及以上人口已近1.8亿,占总人口的12.6%。按照联合国的标准,我国早已进入老龄化社会。更为严峻的是,中国疾病预防控制中心的研究显示,在60岁及以上的老年人群中,高达75.8%的人受到一种或多种慢性病的困扰,且很多人同时患有多种疾病。
这使得许多双独家庭的年轻儿女承受着四位老人的赡养及多种慢病治疗药物的沉重经济负担。
在老龄化趋势日益明显的今天,解决与年龄相关的慢性病问题,以减轻健康和经济负担,已成为当务之急。而目前,科学家们可能已经找到了一个潜在的解决方案——NAD+。
这一被誉为能恢复和维持细胞健康的“奇迹分子”,在动物实验中已展现出对心脏病、糖尿病、阿尔茨海默症和肥胖等多种疾病的治疗潜力。
科学家们对NAD+的研究仍在深入进行中。未来,如果在人类中证实了补充NAD+的安全性和有效性,这将成为解决老年疾病负担、将理想变为现实的关键一步。
参考文献
- https://www.nmn.com/precursors/what-is-nad.
- Massudi H , Grant R , Braidy N , et al. Age-Associated Changes In Oxidative Stress and NAD+ Metabolism In Human Tissue[J]. PLoS ONE, 2012, 7(7).
- Johnson S , Imai, Shin–ichiro. NAD+ biosynthesis, aging, and disease[J]. F1000 Research, 2018, 7.
- Okabe K , Yaku K , Tobe K , et al. Implications of altered NAD metabolism in metabolic disorders[J]. Journal of Biomedical Science, 2019, 26(1).
- Hong W , Mo F , Zhang Z , et al. Nicotinamide Mononucleotide: A Promising Molecule for Therapy of Diverse Diseases by Targeting NAD+ Metabolism[J]. Frontiers in Cell and Developmental Biology, 2020, 8:246.
- Aerobic and resistance exercise training reverses age‐dependent decline in NAD+ salvage capacity in human skeletal muscle[J]. Physiological Reports, 2019, 7(12).
- 王丽敏, 陈志华, 张梅,等. 中国老年人群慢性病患病状况和疾病负担研究[J]. 中华流行病学杂志, 2019, 40(3):7.
- 文章来源:https://www.nmn.cn/nad